OGMinact validation
Afin de valider plus formellement l'inactivation habituelle des OGM réalisée avec de l'eau de Javel pour l'élimination des plaques et des cultures, nous ajoutons cette page. Cette validation a été effectuée avec deux marques d'eau de Javel commerciale et s'applique à la fois aux bactéries OGM et aux vers nématodes transformés avec des plasmides résistants aux antibiotiques. Elle est directement spécifique à cette procédure opératoire standadisée (SOP) de la collection du laboratoire.
Comme toujours, les précautions à prendre lors de l'utilisation de l'eau de Javel et les équipements de protection individuelle appropriés (blouse, gants et protection des yeux) sont des éléments essentiels de cette méthode d'inactivation.
Le grand plateau blanc - étiqueté "Clean Up" - a été utilisé, comme d'habitude, pour toutes les manipulations.
La validation des plaques bactériennes a été faite sur des bactéries transformées avec un plasmide pJAMA-GFP, qui produisent des colonies vertes brillantes...
Une culture fraîche de 2ml a été utilisée pour faire trois plaques de cultures sur des milieux de croissance contenant l'antibiotique sélectif, l'ampicilline (plaques LB-amp100).
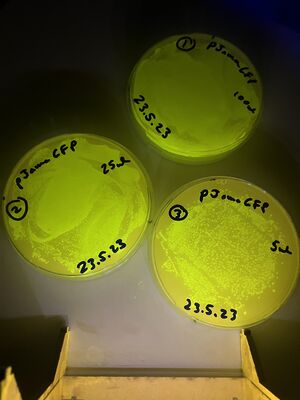
1, avec 100ul de culture (pleinement couverte)
2, avec 25ul de culture (moins de poussé)
3, avec 5ul de culture (encore trop nombreux pour être comptés)
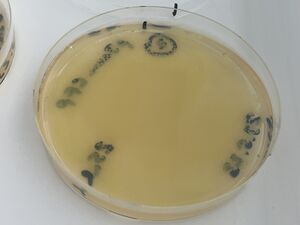
Ces plaques sont montré ci-dessous :
Pour obtenir l'image de fluorescence, nous avons utilisé notre "trans-illuminateur DIY" avec des LED bleues brillantes et un filtre ambre (placé devant l'appareil photo d'un téléphone).
Ensuite, les plaques ont été traitées à dans le grand bac blanc.
Pour cette expérience de validation, trois conditions d'inactivation ont été appliquées : eau de Javel à pleine puissance pour la plaque 1, 1/10 d'eau de Javel dans de l'eau pour la plaque 2, et de l'eau uniquement pour la plaque 3, qui contient le moins de colonies.
5 ml de chaque solution ont été ajoutés à la plaque appropriée, incubés pendant 5 minutes, puis agités, comme indiqué ci-dessous, et incubés pendant 5 minutes supplémentaires.
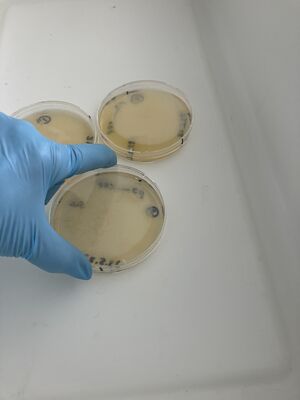
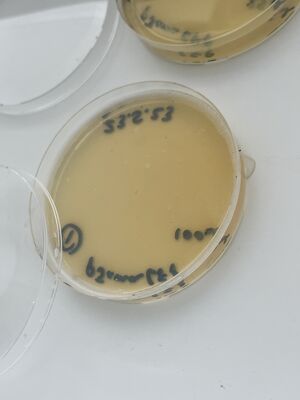
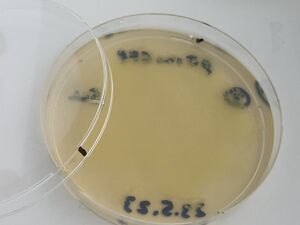
Ensuite, après avoir attendu 5 minutes supplémentaires, quelques ml du liquide de chaque plaque ont été récupérés dans de petits tubes coniques (15 ml) à l'aide de pipettes sérologiques stériles et de la vieille pipette Drummond. Sur la plaque 1, toutes les colonies semblaient complètement dissoutes par l'eau de Javel non diluée, mais la plaque 2 avec 1/10 d'eau de Javel et la plaque 3, avec seulement de l'eau, présentaient encore des colonies intactes, comme montré.
À partir des liquides récupérés, trois autres plaques fraîches ont été réalisées en inoculant 50ul de chaque liquide prélevé après le traitement, comme indiqué.
Après tout cela, on a répété l'inactivation des trois plaques initiales, conformément au mode opératoire normalisé, en ajoutant 100 % de javel sur les plaques 2 et 3 (surtout parce qu'il était clair que même la solution à 1/10 ne dissolvait pas les colonies, comme le fait la solution à pleine puissance). Les liquides ont été inactivés avec de l'eau de Javel fraîche pour être éliminés, et le plateau de nettoyage a été soigneusement lavé dans le grand évier, comme d'habitude (à l'arrière, dans l'espace intermédiaire de Polymeka).
Les 9 nouvelles plaques ont été incubées pendant la nuit à 37oC et leur croissance a été vérifiée.
En fin de compte, l'expérience a très bien validé notre méthode d'inactivation ordinaire, mais nous a réservé quelques surprises.
Aucune colonie n'a été trouvée sur les nouvelles plaques en trois exemplaires, que ce soit pour la première ou la deuxième condition de traitement. Le fait que la condition 2 ait si bien fonctionné, ne donnant pas non plus de colonies sur ces plaques secondaires, puisque les colonies originales ne se sont pas dissoutes avec 1/10 de javel, a été assez surprenant. (En termes de réduction des risques, cependant, il semble toujours préférable d'utiliser de l'eau de Javel à 100 %, comme dans le mode opératoire normalisé). Seul le traitement à l'eau a permis la croissance sur les nouvelles plaques.
Voici une image des 9 plaques, en lumière ordinaire.
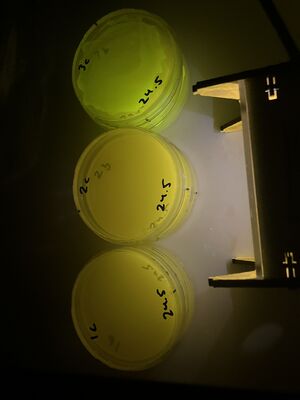
Voici l'image de fluorescence (piles de 3 plaques).
Aucune colonie n'a été observée sur ces plaques secondaires exposées à l'eau de Javel, même à partir du liquide récupéré sur la plaque traitée avec 1/10 d'eau de Javel.
Nous notons dans l'expérience que nous aurions également pu essayer de récupérer des plasmides à partir des liquides traités, mais que ce test supplémentaire ne fournirait des informations très utiles que si de très bonnes cellules compétentes étaient utilisées. (une sorte de gaspillage)
L'absence de croissance de nouvelles colonies, même pour le traitement 1/10, semble tout à fait acceptable...
Enfin, toutes les plaques secondaires ont été inactivées comme d'habitude, conformément au procédure opératoire standardisée, avant d'être jetées à la poubelle pour l'incineration (une dernière photo ici).
Une validation similaire a été effectuée avec des cultures transformées de C. elegans 'worm', à mettre sur une nouvelle page.